Нуклеофил в химии (лат. nucleus «ядро», др.-греч. φιλέω «любить») — реагент, образующий химическую связь с партнером по реакции (электрофилом) по донорно-акцепторному механизму, предоставляя электронную пару, образующую новую связь. Вследствие того, что нуклеофилы отдают электроны, они по определению являются основаниями Льюиса. В роли нуклеофилов теоретически могут выступать все ионы и нейтральные молекулы с неподеленной электронной парой.
Нуклеофил — электроноизбыточный химический реагент, способный взаимодействовать с электронодефицитными соединениями (электрофилами). Примерами нуклеофилов являются анионы (Cl−, Br−, I−) и соединения с неподелённой электронной парой (NH3, H2O).
В ходе реакций замещения или присоединения нуклеофил атакует по месту полного или частичного положительного заряда на электрофиле. Название «нуклеофил» означает «любящий ядро» и отображает эту способность (атомное ядро заряжено положительно). Относительная реакционная способность нуклеофилов называется нуклеофильность. В пределах одного ряда периодической системы более сильные основания (с бóльшим значением pKa сопряженной кислоты) являются лучшими нуклеофилами. В пределах одной группы на нуклеофильность большее влияние оказывает поляризуемость — лёгкость, с которой деформируется электронное облако атома или молекулы. К примеру, в водных растворах иодид-ион I− более нуклеофилен, чем фторид F−.
Амбидентные нуклеофилы имеют два и более реакционных центра. К примеру, тиоцианат-ион SCN− может атаковать электрофил либо атомом серы, либо атомом азота. Реакции галогеноалканов с SCN− часто приводят к образованию смеси RSCN (алкилтиоцианата) и RNCS (алкилизотиоцианата).
Термины «нуклеофил» и «электрофил» были введены в 1929 Кристофером Ингольдом, заменив предложенные ранее (в 1925) Лэпворсом «катионоид» и «анионоид».
Примеры
В показанном ниже примере бимолекулярного нуклеофильного замещения (SN2) атом кислорода гидроксид-иона донирует пару электронов на связывание с атомом углерода в молекуле бромэтана. Связь между атомами углерода и брома разрывается по гетеролитическому механизму: бром принимает оба электрона этой связи и уходит в виде иона Br−. В данной реакции OH− является нуклеофилом, а CH3CH2Br — электрофилом.
В данной реакции атака нуклеофила происходит со стороны, противоположной уходящей группе. Вследствие этого SN2-процессы сопровождаются обращением (инверсией) конфигурации.
Классификация
Нуклеофилы можно классифицировать несколькими способами: по типу орбитали, с которой донируются электроны, и по природе атома, который образует связь.
По типу реагирующей орбитали
В зависимости от природы орбитали, на которой располагались электроны, пошедшие на образование связи с электрофилом, можно выделить:
- π-нуклеофилы (электроны ушли с π-орбитали):
- алкены, диены, алкины;
- аллилсиланы, аллилгерманы, аллилстаннаны;
- алкил- и силиленоловые эфиры;
- ароматические соединения;
- n-нуклеофилы (электроны находились на несвязывающей орбитали — неподелённой электронной паре):
- амины;
- фосфины;
- фосфиты;
- анионы;
- σ-нуклеофилы (электроны ушли с σ-орбитали):
- доноры гидрид-иона H−.
По атому, образующему связь
Углеродные нуклеофилы
Нуклеофилами с реакционным центром на атоме углерода являются:
- алкил- и арилметаллогалиды (например, CH3MgBr, PhMgCl и т. д.) в реакциях Гриньяра, Реформатского, Барбье и др.
- органолитиевые реагенты (PhLi) и анионы терминальных алкинов (HC≡C−Li+);
- енолы и еноляты (RCH=CH−OH и RCH=CH−O−) являются амбидентными нуклеофилами и могут реагировать как по атому углерода в α-положении, так и по атому кислорода. Обычно преобладают реакции по атому углерода (при этом енолят-ионы активнее енолов). Енолы и еноляты часто применяются в реакциях конденсации, например, в альдольной реакции или конденсации Кляйзена.
- другие частицы с полным или частичным отрицательным зарядом на атоме углерода (например, −CH2−NO2).
Азотные нуклеофилы
Примерами азотных нуклеофилов являются аммиак (NH3), органические амины (RNH2, R2NH, R3N) и азиды (R−N3).
Кислородные нуклеофилы
Типичными кислородными нуклеофилами являются вода (H2O), гидроксид-ион (OH−), спирты (ROH) и алкоксиды (RO−). В показанной ниже разновидности реакции Вильямсона сильное основание депротонирует спирт с образованием алкоксида. Атом кислорода затем внутримолекулярно замещает уходящую группу, приводя к образованию эпоксида − трёхчленного гетероцикла с одним атомом кислорода:
Серные нуклеофилы
Серосодержащие соединения обычно являются хорошими нуклеофилами, так как атом серы легко поляризуется, что облегчает передачу электронной пары. Типичные нуклеофилы этого класса — тиолы (RSH) и тиоляты (RS−).
Шкалы нуклеофильности
Известно несколько способов количественного описания реакционной способности нуклеофилов. Приведенные ниже методы основаны на изучении экспериментальных данных о скорости определенных реакций с участием большого количества нуклеофилов и электрофилов. Как правило, реагенты с выраженным альфа-эффектом не включаются в эти корреляции.
Уравнение Свена — Скотта
Уравнение Свена — Скотта было выведено в 1953 году и является первой попыткой количественно описать реакционную способность нуклеофилов в реакциях SN2:
lg ( k k 0 ) = S ⋅ n {displaystyle lg {left({frac {k}{k_{0}}} ight)}=Scdot n}В этом уравнении k — константа скорости реакции стандартного субстрата с данным нуклеофилом, k0 — константа скорости реакции субстрата со стандартным нуклеофилом (водой), S — параметр чувствительности субстрата к изменению нуклеофила (для CH3Br или CH3I S принимается равным 1), n — параметр нуклеофильности (для воды n = 0, табл. 1, 2).
Таким образом, для реакций
CH3I + H2O → CH3OH + HI CH3I + Nuc−H → CH3−Nuc + HIуравнение Свена — Скотта можно записать как
lg ( k C H 3 I , N u c H k C H 3 I , H 2 O ) = n {displaystyle lg {left({frac {k_{CH_{3}I,NucH}}{k_{CH_{3}I,H_{2}O}}} ight)}=n}Уравнение Ричи
Уравнение Ричи было выведено в 1972 году и выражается следующим образом:
lg ( k k 0 ) = N + {displaystyle lg left({frac {k}{k_{0}}} ight)=N^{+}} ,где k 0 {displaystyle k_{0}} — константа скорости реакции стандартного катиона (обычно соли диазония) с со стандартным нуклеофилом (водой) в водной среде, k {displaystyle k} — константа скорости реакции с заданным нуклеофилом, N + {displaystyle N^{+}} — параметр, зависящий от нуклеофила (табл. 3):
Важной особенностью уравнения Ричи является отсутствие параметра чувствительности субстрата (σ в уравнении Свена-Скотта). Таким образом, принимается, что относительная реакционная способность двух нуклеофилов определяется только значением N+ и не зависит от партнера по реакции. Это находится в резком противоречии с т. н. принципом взаимозависимости реакционной способности и селективности. Из-за этого уравнение Ричи иногда называется «соотношение постоянной селективности». Явная упрощенность вызвала ряд публикаций о пределах его применимости.
Уравнение Майра — Патца
В 1994 г. Г. Майр и М. Патц, на основании исследования реакционной способности диарилметильных катионов и других соединений, предложили уравнение, описывающее реакционную способность достаточно большого количества нуклеофилов и электрофилов:
lg k = s ( N + E ) {displaystyle lg k=s(N+E)}В этом уравнении константа скорости реакции второго порядка k, измеренная при 20 °C, связывается с параметром электрофильности E (для бис(п-метоксифенил)метильного катиона E = 0), параметром нуклеофильности N и фактором чувствительности s (для реакций 2-метил-1-пентена s = 1). Для реакций незаряженных нуклеофилов константа скорости слабо зависит от растворителя и последний обычно не указывается.
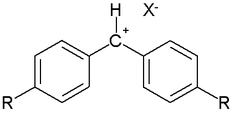
Диарилметильные катионы были выбраны в качестве стандартных электрофилов потому, что их активностью можно управлять подбором заместителя R в пара-положении. Таким образом, оказалось возможным измерить реакционную способность очень разных нуклеофилов. Для протестированных соединений параметр N изменяется в диапазоне от −4,47 до 28,95 (Табл. 4).
Параметр элекрофильности E для некоторых карбокатионов можно грубо оценить по следующему уравнению:
E ≈ 1.241 lg k w − 5.80 {displaystyle Eapprox 1.241lg k_{w}-5.80} ,где kw — константа псевдопервого порядка для реакции карбокатиона с водой при 20 °C.
Нуклеофильность N в уравнении Майра — Патца связана с параметром Ричи N+ следующим соотношением:
N ≈ 1.20 N + + 6.18 {displaystyle Napprox 1.20N_{+}+6.18}Объединенное уравнение
В попытке объединить все вышеописанные уравнения Майр с сотрудниками предложили следующее выражение:
lg k = s E s N ( N + E ) {displaystyle lg k=s_{E}s_{N}(N+E)} ,
где sE — параметр чувствительности электрофила; sN — параметр чувствительности нуклеофила; N и E имеют такое же значение, как и в уравнении Майра — Патца.
С помощью соответствующих подстановок данное выражение можно превратить в любое описанное ранее уравнение:
- при sE = 1 (для карбокатионов) это уравнение эквивалентно оригинальному уравнению Майра — Патца;
- при sN = 0.6 (для большинства n-нуклеофилов):
- при sE = 1 и sN = 0.6 получим: